Todos os isômeros possuem propriedades físicas diferentes, tais como PF, PE e densidade, mas os isômeros ópticos não possuem esta diferença, ou seja, as propriedades físicas dos isômeros ópticos são as mesmas. Então o que faz eles serem diferentes?
É possível diferenciá-los?
Sim, é possível diferenciá-los, mas apenas quando eles estão frente à luz polarizada.
Luz polarizada - é um conjunto de ondas eletromagnéticas que se propagam em apenas uma direção.
Uma lâmpada incandescente é um exemplo de fonte de luz não polarizada, pois a luz é emitida em todas as direções.
É possível polarizar luz não polarizada, bastando utilizar um polarizador, que terá a função de direcionar apenas uma direção da luz.
É possível diferenciá-los?
Sim, é possível diferenciá-los, mas apenas quando eles estão frente à luz polarizada.
Luz polarizada - é um conjunto de ondas eletromagnéticas que se propagam em apenas uma direção.
Uma lâmpada incandescente é um exemplo de fonte de luz não polarizada, pois a luz é emitida em todas as direções.
É possível polarizar luz não polarizada, bastando utilizar um polarizador, que terá a função de direcionar apenas uma direção da luz.
 luz não polarizada luz não polarizada |
esta seta de duas pontas, 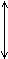 , significa a propagação da onda eletromagnética (luz polarizada) vista de frente.
, significa a propagação da onda eletromagnética (luz polarizada) vista de frente.
Isômeros ópticos
Enantiômeros:
Os isômeros ópticos são compostos capazes de desviar a luz polarizada. Caso o isômero óptico provoque o giro da luz polarizada para a direita, o enantiômero é denominado dextrógiro (D, +). Caso o enantiômero provoque o giro da luz polarizada para a esquerda, o composto é denominado levógiro (L, -).
É necessário atenção, pois os enantiômeros não são superponíveis, assim como o levógiro não se superpõe ao dextrógiro.
O fato de um composto provocar o "giro" da luz polarizada, faz com que ele possua atividade óptica.
Atividade óptica só é possível em moléculas assimétricas, ou seja, moléculas que possuem carbono quiral (ou estereocentro).
Isômeros ópticos
Enantiômeros:
Os isômeros ópticos são compostos capazes de desviar a luz polarizada. Caso o isômero óptico provoque o giro da luz polarizada para a direita, o enantiômero é denominado dextrógiro (D, +). Caso o enantiômero provoque o giro da luz polarizada para a esquerda, o composto é denominado levógiro (L, -).
É necessário atenção, pois os enantiômeros não são superponíveis, assim como o levógiro não se superpõe ao dextrógiro.
O fato de um composto provocar o "giro" da luz polarizada, faz com que ele possua atividade óptica.
Atividade óptica só é possível em moléculas assimétricas, ou seja, moléculas que possuem carbono quiral (ou estereocentro).
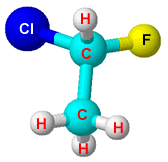 | o carbono quiral é marcado com um asterísco (*),este carbono possui todos os ligantes diferentes. |
 |  | 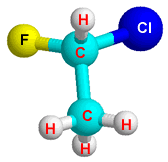 |
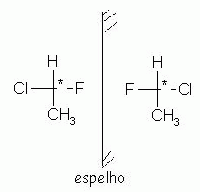 |
Compostos enantioméricos, um é a imagem especular do outro, ou seja, um é a imagem refletida do outro. No entanto, eles não são superponíveis. Um exemplo disso, são as mãos, direita e esquerda. Uma é a imagem da outra, mas não são superponíveis. Tente verificar este fato com suas mãos, coloque uma na frente da outra. (Uma será a imagem da outra).
Agora tente colocar uma sobre a outra. (As mãos não são superponíveis, ou seja, os dedos polegares não ficam um sobre o outro). Considere isso como um exemplo para entender o fato da assimetria molecular.
Mistura racêmica é uma mistura de isômeros ópticos, ou seja, é uma mistura de 50% de levógiro e 50% de dextrógiro.
A quantidade de isômeros opticamente ativos, pode ser dada a partir da quantidade de carbonos quirais em uma molécula.
Agora tente colocar uma sobre a outra. (As mãos não são superponíveis, ou seja, os dedos polegares não ficam um sobre o outro). Considere isso como um exemplo para entender o fato da assimetria molecular.
Mistura racêmica é uma mistura de isômeros ópticos, ou seja, é uma mistura de 50% de levógiro e 50% de dextrógiro.
A quantidade de isômeros opticamente ativos, pode ser dada a partir da quantidade de carbonos quirais em uma molécula.
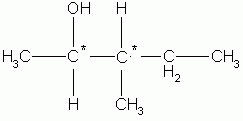
2 estereocentros
IOA- isômero óticamente ativo
IOA = 2n , sendo n o número de estereocentros.
Para a molécula dada, temos:
IOA = 22 = 4 , 4 isômeros ópticos ativos
IOA = 2n , sendo n o número de estereocentros.
Para a molécula dada, temos:
IOA = 22 = 4 , 4 isômeros ópticos ativos
*O texto e as figuras desta página foram produzidos por Miguel A. Medeiros. A reprodução destes, merece autorização ou referência ao autor. Além do endereço desta página. www.quiprocura.net
Nenhum comentário:
Postar um comentário